Project Description
临床上根据肿瘤大小 (T)、淋巴腺转移状态 (N)、 远处转移与否 (M) 的 TNM 分期源于 1959 年,长久来 一直是乳癌分期 ( 包括临床、病理分期 ) 的主流,也得 以预测病人预后及作为治疗的根据。然而,由于临床、 实验科学、转译医学的进步,让我们对乳癌的面像有更 清楚的认知与了解,如生物标记雌激素受体 (Estrogen Receptor;ER)、 黄 体 素 受 体 (Progesterone Receptor; PR)、 第 二 型 人 类 上 皮 细 胞 生 长 因 子 受 体 (Human Epidermal growth factor Receptor 2;HER-2),不仅扮演 着预后角色,同时也扮演着选择有效药物治疗的角色; 上述生物标记的长足进步也使得乳房医学界对乳癌的 治疗已经跨出仅限于考虑 TNM 的时代。美国癌症联合 委 员 会 (American Joint Committee on Cancer;AJCC) 于 AJCC 第八版中将肿瘤恶性度、ER、PR、HER-2 及 基因检验结果结合了 TNM 分期法而将乳癌分期划分有 ①解剖分期 (Anatomic Stage):主要基于 TNM 的临床解 剖影响范围为分期②临床预后分期 (Clinical Prognostic Stage):基于理学检查、影像检查、切片结果而划分。 由 TNM、肿瘤恶性级数、ER、PR、 HER-2 数据加以分 期③病理预后分期 (Pathological Prognostic Stage):适 用于以手术为第一时间治疗方式的对象,分期根据有临 床信息、生物标记数据、手术切除检体的发现。此分期 法比较适合使用于美国国度及高医疗水平国家,因为它 含括有基因检测结果的要项。
◎美国癌症联合委员会 (AJCC) 第八版主要有哪些数据的更新?
- 1. 乳小叶原位癌(Lobular Carcinoma In Situ;LCIS不再归类于原位乳癌(pTis),将LCIS视为良性疾病本质而不再归分于T、N、M 分期。
2. 皮肤上的卫星肿瘤结节(Satellite tumor nodules),如无皮肤溃疡存在,则不视为T4b而以实际肿瘤大小为登录。
3. pM0不是具信效度的登录,若有转移处病理组织的确认才能登录为pM1,否则就记录为cM0(临床无转移)或cM1(临床有转移)。
4. 完全病理反应(pCR)定义为无发现残留侵袭病灶于乳腺、淋巴腺或淋巴血管中。
5. 基因检测并非必要登录项目,虽然它可提供治疗、预后信息。
6. 安可待基因检测(Oncotype Dx)复发分数<11者无论其肿瘤大小 (T 期数 ) 归类为 T1a-T1bN0M0。Oncotype Dx 检测对象为肿瘤<5公分、荷尔蒙受体阳性、淋巴腺未转移、HER-2 阴性。目前市面上常见基因检测平台如:① Breast Cancer Index ② Endopredict③ Mammaprint ④ PAM-50(Prosigna) 等只要结果是低复发风险者也归类为 T1a-T1bN0M0;此些多基因检测对象者也如上述 Oncotype Dx 般,如果肿瘤 <5 公分、荷尔蒙体阳性、淋巴腺未转移、HER-2 阴性,只要低复发风险分数者也归类于T1a-T1bN0M0 的分期。结论为多基因检测结果不管肿瘤大小,只要低复发风险分数者,因为其预后极佳,给予归类于 T1a-T1bN0M0 的分期。惟上述多种基因检测法中只有安可待基因检测(Oncotype Dx)被第八版AJCC认定为第一级证据(Level 1 evidence)。
◎多基因检测平台的临床发展与应用
虽然 T、N、M 分类法仍然是提供临床预后的主流, 但是现今医师必须将生物标记 (ER、PR、HER-2、Ki67、Grade) 及可能的话也把基因检测结果共列为治疗决 策。目前世界上仍然不乏存在许多国家无法将生物标记 进一步检测更遑论基因检测平台,因此 T、N、M 的基 本分期依然普遍适用于中低收入国家。
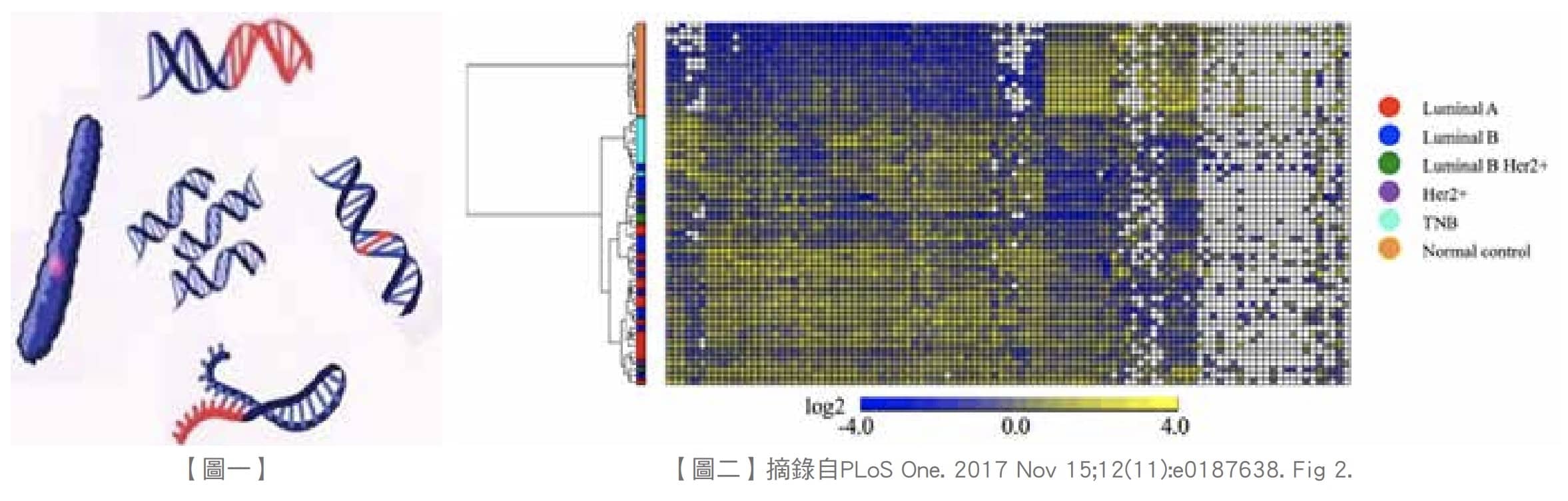
传统以病理为基础的预后因子无法完全解释乳癌长 期存活与临床预后的差异,因此多基因预后标记的发展 可以补强病理报告之不足,乳癌基因检测 ( 图一 ) 可作 为乳癌预测预后及治疗用途,部分检测平台已经商品化 而且已列入重要国际学会的临床指引,作为乳癌治疗方 针的参考指南。
过去十年藉由微数组 (microarray) 芯片分析 乳 癌 基 因 表 现 的 进 展,目前依照特定基因转录体 表 现 的 型 态,将乳癌区分为管腔 A 型、管腔 B 型、类基 底型与 HER2 扩增型这四种分子亚型 ( 图二 ) 各种亚型 有其治疗建议及预后意义。
- 安可待 (Oncotype DX)
透过使用 21 个基因,并以 PCR 的方式来计算石蜡 包埋检体中的基因表现量,分别于 2015、2018 年发表于新英格兰医学杂志的 TAILORx 研究收案 10273 名乳癌病 人为 HR 阳性、HER2 阴性、淋巴腺无转移者,次 分 组 分 析 显 示复发评分值 (Recurrence Score ) 0-10 分属低 复发风险者,若仅接受抗荷尔蒙治疗而没使用化学治疗 经五年追踪的结果,没有发生远程转移超过 99%,总存 活率 98% ( 第一级证据 ),显示低复发评分者可以避免 化学治疗仅使用荷尔蒙治疗就有极佳的五年存活率。
Recurrence Score 11-25 分 者 ( 中 复 发 风 险 ) 被 随 机分派化学治疗 – 荷尔蒙治疗及仅有荷尔蒙治疗组, 结果仅用荷尔蒙治疗组并不会比化学治疗 – 荷尔蒙治 疗组差。然而必须指出,对于 50 岁以下的年轻女性 Recurrence Score 在 16-25 之间者,化学治疗可能会有所 帮助,值得慎思。Recurrence Score> 26分者(高复发风险) 须接受化学治疗。
综合 TAILORx 研究结果指出,HR 阳性、HER2 阴性、 淋巴腺无转移,可以避免化学治疗约占 70% 的病人。
● 不必接受化学治疗的条件如下: 1) 年龄大于 50 岁且复发评分值为 11~25 2) 不管年龄,复发评分值为 0~10 3) 年龄小于 50 岁,复发评分值为 11~15
● 在 HR 阳性、HER2 阴性、淋巴腺无转移病人中, 仍有 30%病人需要接受化学治疗,条件如下: 1) 任何年龄复发评分值为 26~100 分 2) 50 岁或以下,复发评分值为 16~25 分
- Mammaprint
以微数组技术 (microarray) 分析 70 个基因的表现,针对五年内的复发做风险评估,并区分为高低风险两组;乳癌肿瘤属于高风险,需要接受手术后的辅助化学
治疗,若是低风险,可避免不必要的化疗。Mammaprint 有一个大型随机试验 MINDACT,对象为淋巴腺1-3颗转移的病人。受试者同时以Adjuvant Online评估其临床风险(C)与70-gene的基因表现检测风险(G)。当C/G皆为低风险时就不需化学治疗,当C/G皆为高风险时就要化学治疗。但是当C与G分组不一致时(C高G低或C低G高)则随机分派是否化学治疗,若受试者为荷尔蒙受体阳性,则接受荷尔蒙辅以微数组技术 (microarray) 分析 70 个基因的表现,针对五年内的复发做风险评估,并区分为高低风险两组;乳癌肿瘤属于高风险,需要接受手术后的辅助化学治疗,若是低风险,可避免不必要的化疗。Mammaprint 有一个大型随机试验MINDACT,对象为淋巴腺 1-3 颗转移的病人。受试者同时以Adjuvant Online评估其临床风险(C)与70-gene的基因表现检测风险(G)。当C/G皆为低风险时就不需化学治疗,当C/G皆为高风险时就要化学治疗。但是当C与G分组不一致时(C高G低或C低G高 )则随机分派是否化学治疗,若受试者为荷尔蒙受体阳性,则接受荷尔蒙辅助治疗。主要目的是看临床风险高但基因检测风险低的族群,共有644人没有接受化疗,五年后的无远程
转移存活是94.7%。也因此在2017年美国临床肿瘤医学会(ASCO)发表 Mammaprint 的临床应用指南更新 1)Mammaprint 试验的结果可以被认为是对荷尔蒙受体阳性,HER2阴性,淋巴腺阴性乳腺癌患者的辅助全身化学治疗的决定。2) Mammaprint 也可用于荷尔蒙受体阳性,HER2 阴性乳癌,但淋巴腺有 1-3 颗转移的病人(具有高度复发临床风险的女性)做为决定是否需要辅助化学治疗的决策工具。
- Endo-predict
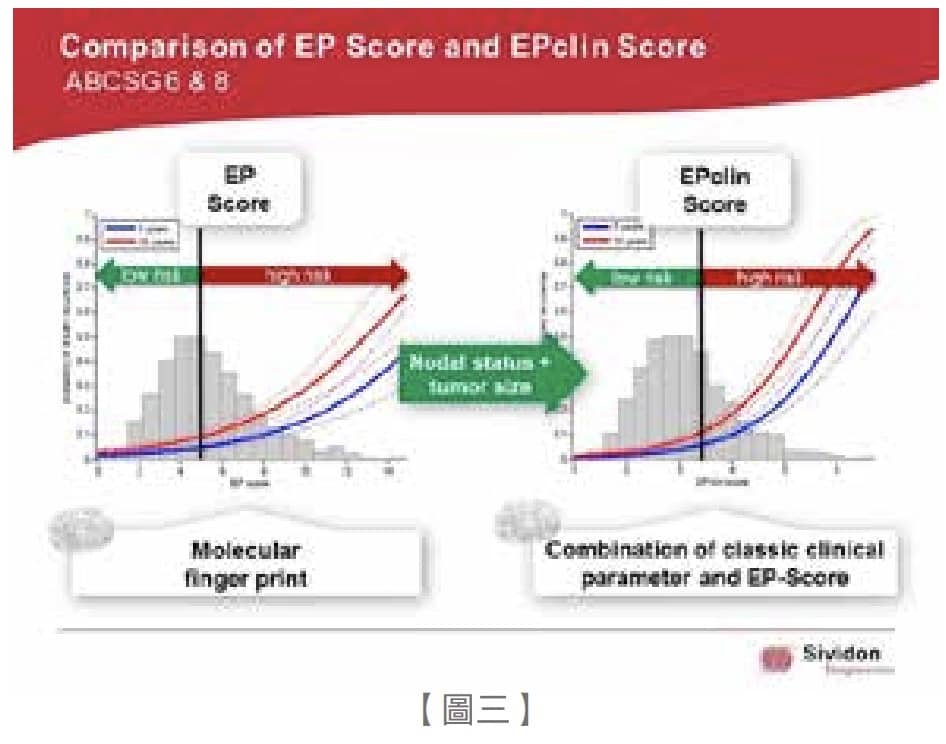
利用实时基因表现侦测技术 (Real-Time PCR),发展自ABCSG6/8临床试验(图三),针对荷尔蒙受体阳性,HER2阴性且淋巴腺转移1~3颗的族群,作为预测术后5-10年是否会远程转移的多基因表现检测。EPScore大于5分或 EPclin Score(考虑肿瘤大小与淋巴转移数目)大于3.3分就算高风险,否则就是低风险族群。
Endo-predict 的好处为报告没有中风险的分类而让人会不知该进行何种辅助性治疗 ? 另外可以在国内进行检测试验,报告能于 7 天内取得,有其便利性。不像前述几种多基因标记都需要送出国外检验 (Oncotype Dx送美国,Mammaprint送荷兰),对于掌握术后开始化学治疗的黄金效期有其优势。目前乳癌的多基因标记是可以加强分析危险分级及治疗建议参考但并不能取代传统的ER、PR 与 HER2 标记。